BioNTech 公司,作為全球第一家 mRNA 疫苗公司,自 2008 年成立以來就致力于開發(fā)基于 mRNA 的癌癥疫苗。然而,新冠疫情的爆發(fā),讓 mRNA 疫苗后起之秀 Moderna 迅速崛起,市值遠(yuǎn)超 BioNTech,甚至一度接近 2000 億美元。
隨著疫情的結(jié)束,兩家 mRNA 疫苗公司股價(jià)持續(xù)下跌,在 2024 年 9 月 13 日,BioNTech 市值反超了 Moderna,并一直領(lǐng)先至今。目前,BioNTech 市值 287 億美元,是 Moderna 136 億美元的 2 倍多。這在很大程度上得益于 BioNTech 在癌癥疫苗領(lǐng)域的持續(xù)投入和產(chǎn)出。僅在這個(gè)月,BioNTech 就在 Nature 期刊發(fā)表了兩篇論文,分別展示了個(gè)性化新抗原癌癥疫苗在腎細(xì)胞癌和
2025 年 2 月 19 日,BioNTech 公司聯(lián)合紀(jì)念斯隆凱特琳癌癥中心的研究人員,在國(guó)際頂尖學(xué)術(shù)期刊 Nature 上發(fā)表了題為:RNA neoantigen vaccines prime long-lived CD8+ T cells in pancreatic cancer 的研究論文。
該研究表明,mRNA 新抗原疫苗在胰腺導(dǎo)管腺癌(PDAC)患者中誘導(dǎo)了具有長(zhǎng)壽命、顯著規(guī)模和持久效應(yīng)功能的 CD8+ T 細(xì)胞,從而有效降低了癌癥復(fù)發(fā)風(fēng)險(xiǎn)。該研究展示了 mRNA 新抗原疫苗在胰腺癌治療中的潛力,通過誘導(dǎo)長(zhǎng)效、功能性的 T 細(xì)胞反應(yīng),可能為癌癥免疫治療帶來新策略。

胰腺癌,其最常見類型為胰腺導(dǎo)管腺癌(PDAC),是一類極度致命的惡性腫瘤,具有很高的死亡率,80%-85% 的患者在確診時(shí)已處于晚期或已出現(xiàn)轉(zhuǎn)移。近年來,全世界的研究人員付出了巨大努力來開發(fā)新型治療策略和治療組合以改善胰腺癌患者的治療效果,但其死亡率仍然居高不下,5 年生存率不足 10%,因此也被稱為“癌癥之王”。
胰腺導(dǎo)管腺癌(PDAC)具有較低的突變負(fù)荷,因此傳統(tǒng)的免疫療法效果有限。BioNTech 公司開發(fā)了一款名為 Autogene cevumeran 的個(gè)性化 mRNA 新抗原疫苗,這是一款 mRNA 經(jīng)過優(yōu)化修飾的 mRNA-LNP 疫苗,旨在通過引發(fā)針對(duì)腫瘤特異性新抗原的 T 細(xì)胞反應(yīng)來增強(qiáng)胰腺導(dǎo)管腺癌的免疫治療效果。
在這項(xiàng) 1 期臨床試驗(yàn)中,研究團(tuán)隊(duì)納入了 19 名已接受手術(shù)切除的胰腺導(dǎo)管腺癌患者。治療方案包括:
1、手術(shù)治療:切除腫瘤;
2、Atezolizumab(抗 PD-L1 單抗):?jiǎn)未蝿┝浚糜谝种?PD-L1 通路;
3、Autogene cevumeran:個(gè)性化 mRNA 新抗原疫苗,包含最多 20 個(gè) MHC I 類和 II 類限制性新抗原,通過靜脈注射進(jìn)行 8 次初始劑量和 1 次加強(qiáng)劑量注射;
4、mFOLFIRINOX 化療:12個(gè)周期的化療。
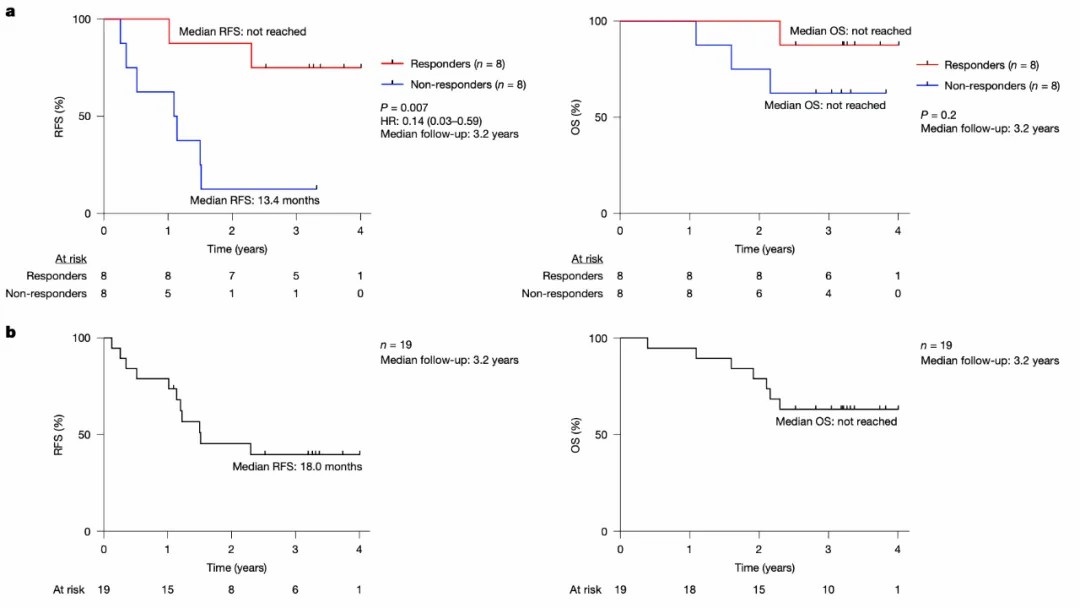
結(jié)果顯示:在為期 3.2 年的中位隨訪期間,未產(chǎn)生疫苗誘導(dǎo) T 細(xì)胞應(yīng)答的非應(yīng)答者(n=8)的中位無復(fù)發(fā)生存期(RFS)為 13.4 個(gè)月;產(chǎn)生疫苗誘導(dǎo) T 細(xì)胞應(yīng)答的應(yīng)答者(n=8)的 RFS 顯著延長(zhǎng)(該論文發(fā)表時(shí),中位值尚未達(dá)到),其中 6 位患者無復(fù)發(fā)。與無應(yīng)答者相比,應(yīng)答者的癌癥復(fù)發(fā)風(fēng)險(xiǎn)降低了 86%。
在應(yīng)答者中,疫苗誘導(dǎo)的 CD8+T 細(xì)胞克隆平均預(yù)計(jì)壽命長(zhǎng)達(dá) 7.7 年(范圍在 1.5 年至約 100 年),其中約 20% 克隆具有潛在的數(shù)十年壽命(可能超過宿主壽命)。疫苗接種約 3 年后,每位患者中 86% 的克隆仍以顯著頻率持續(xù)存在,包括對(duì) PDAC 新表位具有高親和力的克隆。通過新型計(jì)算策略 PhenoTrack(追蹤單T細(xì)胞表型)發(fā)現(xiàn):疫苗誘導(dǎo)的克隆在接種前組織中無法檢測(cè)到,且在接種后三年內(nèi)持續(xù)處于細(xì)胞毒性、組織駐留記憶樣 T 細(xì)胞狀態(tài),并保持新抗原特異性效應(yīng)功能。在 2 位出現(xiàn)癌癥復(fù)發(fā)的應(yīng)答者中,疫苗誘導(dǎo)的 T 細(xì)胞數(shù)量較少,且復(fù)發(fā)性 PDAC 中疫苗靶向的腫瘤克隆被清除。
總的來說,這項(xiàng)臨床試驗(yàn)表明,個(gè)性化 mRNA 新抗原疫苗 Autogene cevumeran 在胰腺導(dǎo)管腺癌(PDAC)患者中誘導(dǎo)了具有長(zhǎng)壽命、顯著規(guī)模和持久效應(yīng)功能的 CD8+ T 細(xì)胞,從而有效降低了癌癥復(fù)發(fā)風(fēng)險(xiǎn),表明了基于 mRNA 的新抗原疫苗可能攻克癌癥疫苗關(guān)鍵瓶頸。
相關(guān)閱讀:
2025 年 2 月 5 日,BioNTech 公司聯(lián)合耶魯大學(xué)醫(yī)學(xué)院、哈佛大學(xué)醫(yī)學(xué)院 Dana-Farber 癌癥研究所等機(jī)構(gòu)的研究人員,在國(guó)際頂尖學(xué)術(shù)期刊 Nature 上發(fā)表了題為:A neoantigen vaccine generates antitumour immunity in renal cell carcinoma 的研究論文。
在這項(xiàng) 1 期臨床試驗(yàn)中,9 例高危腎細(xì)胞癌患者接受了新抗原靶向的個(gè)性化癌癥疫苗治療。結(jié)果顯示,疫苗在所有患者中都產(chǎn)生了抗腫瘤免疫反應(yīng),盡管這些患者都具有癌癥復(fù)發(fā)的高風(fēng)險(xiǎn),但在超過 3 年(40個(gè)月)的研究期間沒有一個(gè)人出現(xiàn)癌癥復(fù)發(fā),突顯了個(gè)性化癌癥疫苗作為腎細(xì)胞癌有效輔助治療的前景。

論文鏈接:
https://www.nature.com/articles/s41586-024-08508-4
https://www.nature.com/articles/s41586-024-08507-5
來源:生物世界